PRP مدرن: "پی آر پی بالینی"
در 10 سال گذشته، طرح درمان PRP دستخوش تغییرات بزرگی شده است.از طریق تحقیقات تجربی و بالینی، ما اکنون درک بهتری از پلاکت و سایر فیزیولوژی سلولی داریم.علاوه بر این، چندین ارزیابی سیستماتیک با کیفیت بالا، متاآنالیزها و کارآزماییهای تصادفیسازی شده کنترلشده اثربخشی بیوتکنولوژی PRP را در بسیاری از زمینههای پزشکی از جمله پوست، جراحی قلب، جراحی پلاستیک، جراحی ارتوپدی، مدیریت درد، بیماریهای ستون فقرات و پزشکی ورزشی نشان دادهاند. .
مشخصه فعلی PRP غلظت مطلق پلاکت آن است که از تعریف اولیه PRP (شامل غلظت پلاکت بالاتر از مقدار پایه) به بیش از 1 × 106/μL یا حدود 5 برابر حداقل غلظت پلاکتی در پلاکت ها تغییر می کند. خط پایهدر بررسی گسترده فدادو و همکاران.33 سیستم و پروتکل PRP مورد ارزیابی قرار گرفت.تعداد پلاکت های آماده سازی نهایی PRP که توسط برخی از این سیستم ها تولید می شود کمتر از خون کامل است.آنها گزارش دادند که فاکتور پلاکتی PRP با کیت تک چرخشی (Selphyl®) تا 0.52 افزایش یافت.در مقابل، دو چرخش EmCyte Genesis PurePRPII® غلظت پلاکت تولید شده توسط دستگاه بالاترین (1.6 × 106 /µL) است.
بدیهی است که روش های آزمایشگاهی و حیوانی محیط تحقیقاتی ایده آل برای تبدیل موفقیت آمیز به عمل بالینی نیستند.به طور مشابه، مطالعه مقایسه دستگاه ها از این تصمیم پشتیبانی نمی کند، زیرا آنها نشان می دهند که غلظت پلاکت بین دستگاه های PRP بسیار متفاوت است.خوشبختانه، از طریق فناوری و تجزیه و تحلیل مبتنی بر پروتئومیکس، میتوانیم درک خود را از عملکرد سلولی در PRP افزایش دهیم که بر نتایج درمان تأثیر میگذارد.قبل از رسیدن به اجماع در مورد آماده سازی و فرمولاسیون استاندارد PRP، PRP باید از فرمولاسیون PRP بالینی پیروی کند تا مکانیسم های قابل توجه ترمیم بافت و نتایج بالینی پیشرونده را ارتقا دهد.
فرمول PRP بالینی
در حال حاضر، PRP بالینی موثر (C-PRP) به عنوان ترکیب پیچیده ای از اجزای چند سلولی اتولوگ در پلاسمای با حجم کم که از بخشی از خون محیطی پس از سانتریفیوژ به دست می آید، مشخص شده است.پس از سانتریفیوژ، PRP و اجزای سلول غیر پلاکتی آن را می توان از دستگاه غلظت با توجه به تراکم سلولی مختلف (که تراکم پلاکتی کمترین آن است) بازیابی کرد.
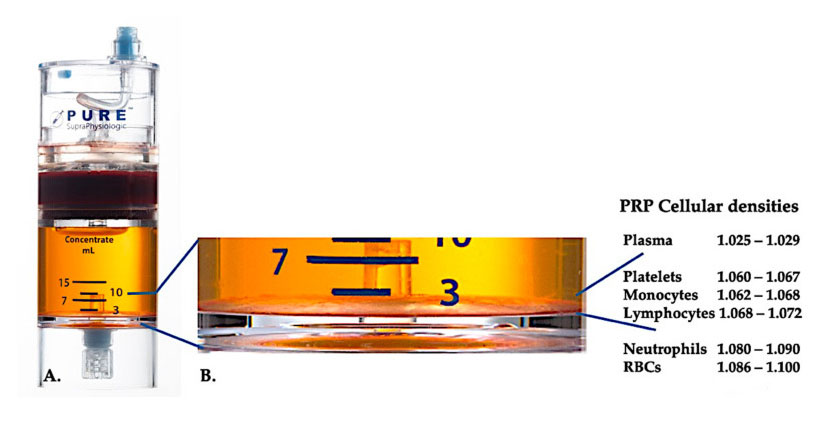
استفاده از تجهیزات جداسازی تراکم سلولی PurePRP-SP® (EmCyte Corporation، Fort Myers، FL، USA) پس از دو روش سانتریفیوژ برای خون کامل استفاده شد.پس از اولین فرآیند سانتریفیوژ، اجزای خون کامل به دو لایه اساسی، سوسپانسیون پلاسمای پلاکتی (لاغر) و لایه گلبول قرمز جدا شد.در A، مرحله دوم سانتریفیوژ کامل شده است.حجم واقعی PRP را می توان برای استفاده بیمار استخراج کرد.بزرگنمایی در B نشان می دهد که یک لایه قهوه ای ته نشینی گلبول قرمز چند جزئی (که با خط آبی نشان داده می شود) در پایین تجهیزات وجود دارد که حاوی غلظت بالایی از پلاکت ها، مونوسیت ها و لنفوسیت ها بر اساس گرادیان چگالی است.در این مثال، طبق پروتکل آماده سازی C-PRP با نوتروفیل های ضعیف، حداقل درصد نوتروفیل ها (<0.3٪) و گلبول های قرمز (<0.1٪) استخراج می شود.
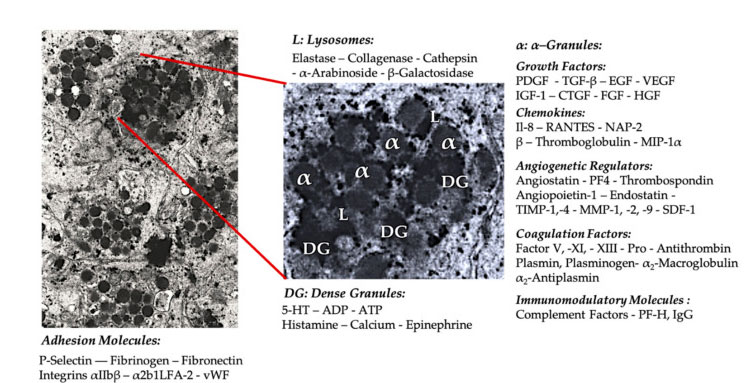
گرانول پلاکتی
در کاربردهای اولیه PRP بالینی، گرانولهای α رایجترین ساختار داخلی پلاکتی هستند، زیرا حاوی فاکتورهای انعقادی، تعداد زیادی PDGF و تنظیمکنندههای رگزایی هستند، اما عملکرد ترومبوژنیک کمی دارند.عوامل دیگر عبارتند از کموکاین و اجزای سیتوکین کمتر شناخته شده، مانند فاکتور پلاکت 4 (PF4)، پروتئین پایه پیش پلاکتی، P-سلکتین (فعال کننده اینتگرین) و کموکین RANTES (تنظیم شده توسط فعال سازی، بیان سلول های T طبیعی و احتمالاً ترشح می کند).عملکرد کلی این اجزای گرانول پلاکتی خاص جذب و فعال کردن سایر سلول های ایمنی یا القای التهاب سلول های اندوتلیال است.
اجزای دانه ای متراکم مانند ADP، سروتونین، پلی فسفات، هیستامین و آدرنالین به طور ضمنی به عنوان تنظیم کننده فعال شدن پلاکت و ترومبوز استفاده می شوند.مهمتر از همه، بسیاری از این عناصر عملکرد اصلاح سلول های ایمنی را دارند.ADP پلاکتی توسط گیرنده P2Y12ADP بر روی سلول های دندریتیک (DC) شناسایی می شود و در نتیجه اندوسیتوز آنتی ژن را افزایش می دهد.DC (سلول ارائه دهنده آنتی ژن) برای شروع پاسخ ایمنی سلول T و کنترل پاسخ ایمنی محافظتی، که سیستم ایمنی ذاتی و سیستم ایمنی تطبیقی را به هم پیوند می دهد، بسیار مهم است.علاوه بر این، آدنوزین تری فسفات پلاکتی (ATP) سیگنال هایی را از طریق گیرنده سلول T P2X7 ارسال می کند که منجر به افزایش تمایز سلول های کمکی CD4 T به سلول های T helper 17 (Th17) پیش التهابی می شود.سایر اجزای گرانول متراکم پلاکتی (مانند گلوتامات و سروتونین) به ترتیب باعث مهاجرت سلول های T و افزایش تمایز مونوسیت ها به DC می شوند.در PRP، این تعدیل کننده های ایمنی مشتق شده از ذرات متراکم بسیار غنی شده و عملکردهای ایمنی قابل توجهی دارند.
تعداد فعل و انفعالات بالقوه مستقیم و غیرمستقیم بین پلاکت ها و سایر سلول های (گیرنده) زیاد است.بنابراین، استفاده از PRP در محیط بافت پاتولوژیک موضعی میتواند باعث ایجاد انواع اثرات التهابی شود.
غلظت پلاکت
C-PRP باید حاوی دوزهای بالینی پلاکت های غلیظ باشد تا اثرات درمانی مفیدی ایجاد کند.پلاکتهای موجود در C-PRP باید تکثیر سلولی، سنتز فاکتورهای مزانشیمی و نوروتروفیک را تحریک کنند، مهاجرت سلولهای کموتاکتیک را تقویت کنند و فعالیت تنظیمکننده ایمنی را تحریک کنند، همانطور که در شکل نشان داده شده است.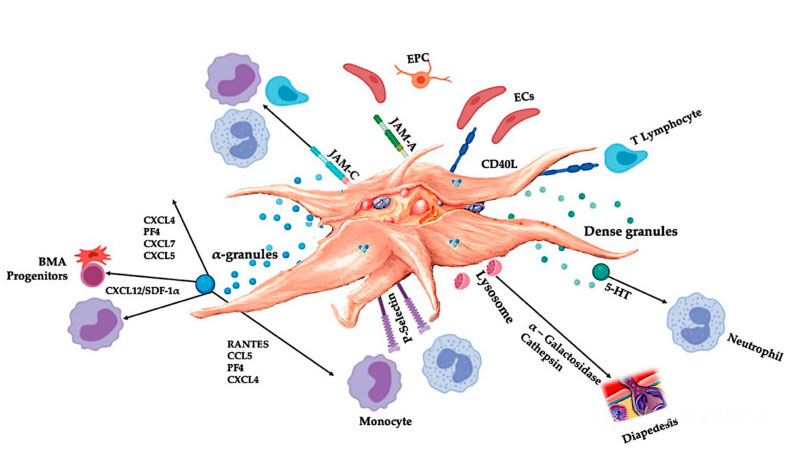
پلاکتهای فعال شده، آزادسازی PGF و مولکولهای چسبنده، میانجی انواع برهمکنشهای سلولی هستند: کموتاکسی، چسبندگی سلولی، مهاجرت و تمایز سلولی، و فعالیتهای تنظیمی ایمنی را تنظیم میکنند.این فعل و انفعالات سلول-سلول پلاکتی به رگزایی و فعالیت التهابی کمک می کند و در نهایت فرآیند ترمیم بافت را تحریک می کند.مخفف ها: BMA: آسپیرات مغز استخوان، EPC: سلول های پیش ساز اندوتلیال، EC: سلول های اندوتلیال، 5-HT: 5-هیدروکسی تریپتامین، RANTES: تنظیم فعال بیان سلول های T طبیعی و ترشح احتمالی، JAM: نوع مولکول چسبندگی اتصال، csterlu: CD40L: لیگاند 40، SDF-1 α: فاکتور 1 α مشتق از سلول استرومایی، لیگاند CXCL: کموکاین (موتیف CXC)، PF4: فاکتور پلاکتی 4. اقتباس شده از Everts و همکاران.
مارکس اولین کسی بود که ثابت کرد بهبود استخوان و بافت نرم افزایش یافته است و حداقل تعداد پلاکتها 1 × 10 6 /µL بود. 1.3 × در 106 پلاکت در میکرولیتر، این مطالعه همجوشی بیشتری را نشان داد.علاوه بر این، Giusti و همکاران.مکانیسم ترمیم بافت در دوز 109 به پلاکت در میلی لیتر برای القای آنژیوژنز عملکردی از طریق فعالیت سلول های اندوتلیال نیاز دارد.در مطالعه اخیر، غلظت های بالاتر پتانسیل رگزایی پلاکت ها را در داخل و اطراف فولیکول ها کاهش داد.علاوه بر این، داده های قبلی نشان داد که دوز PRP نیز بر نتایج درمان تأثیر می گذارد.بنابراین، به منظور القای قابل توجه واکنش رگ زایی و تحریک تکثیر سلولی و مهاجرت سلولی، C-PRP باید حاوی حداقل 7.5 در یک بطری 5 میلی لیتری PRP × 109 باشد که بتواند پلاکت ها را تحویل دهد.
علاوه بر وابستگی به دوز، به نظر می رسد اثر PRP بر فعالیت سلولی بسیار وابسته به زمان باشد.سوفی و همکاراناین نتایج نشان می دهد که قرار گرفتن در معرض کوتاه مدت با لیزات پلاکت انسانی می تواند تکثیر سلول های استخوانی و کموتاکسی را تحریک کند.در مقابل، قرار گرفتن طولانی مدت در معرض PRP منجر به کاهش سطح آلکالین فسفاتاز و تشکیل مواد معدنی می شود.
گلبول قرمز
گلبول های قرمز وظیفه انتقال اکسیژن به بافت ها و انتقال دی اکسید کربن از بافت ها به ریه ها را بر عهده دارند.آنها هسته ندارند و از مولکول های هم تشکیل شده اند که به پروتئین ها متصل می شوند.اجزای آهن و هِم موجود در گلبول های قرمز، ترکیب اکسیژن و دی اکسید کربن را تقویت می کنند.به طور کلی، چرخه زندگی گلبول های قرمز حدود 120 روز است.آنها توسط ماکروفاژها از طریق فرآیندی به نام پیری RBC از گردش خون خارج می شوند.گلبولهای قرمز در نمونههای PRP ممکن است تحت شرایط برشی آسیب ببینند (به عنوان مثال، جراحی خونریزی از خون کامل، فرآیند با واسطه سیستم ایمنی، استرس اکسیداتیو یا طرح غلظت ناکافی PRP).بنابراین، غشای سلولی RBC تجزیه شده و هموگلوبین سمی (Hb) را آزاد می کند که با هموگلوبین بدون پلاسما (PFH)، هم و آهن اندازه گیری می شود.].PFH و محصولات تخریب آن (هم و آهن) به طور مشترک منجر به اثرات مضر و سیتوتوکسیک روی بافت ها می شود که منجر به استرس اکسیداتیو، از دست دادن اکسید نیتریک، فعال شدن مسیرهای التهابی و سرکوب سیستم ایمنی می شود.این اثرات در نهایت منجر به اختلال در عملکرد میکروسیرکولاسیون، انقباض عروق موضعی و آسیب عروقی و همچنین آسیب جدی به بافت خواهد شد.
مهمترین چیز این است که وقتی RBC حاوی C-PRP به بافت منتقل می شود، واکنش موضعی به نام اریپتوز ایجاد می کند که باعث آزاد شدن یک مهارکننده موثر سیتوکین و مهاجرت ماکروفاژ می شود.این سیتوکین از مهاجرت مونوسیت ها و ماکروفاژها جلوگیری می کند.این سیگنالهای پیشالتهابی قوی را به بافتهای اطراف ارسال میکند، مهاجرت سلولهای بنیادی و تکثیر فیبروبلاست را مهار میکند و منجر به اختلال عملکرد سلولی محلی میشود.بنابراین، محدود کردن آلودگی RBC در آماده سازی PRP مهم است.علاوه بر این، نقش گلبول های قرمز خون در بازسازی بافت هرگز مشخص نشده است.سانتریفیوژ و فرآیند آماده سازی کافی C-PRP معمولاً حضور گلبول های قرمز را کاهش می دهد یا حتی از بین می برد، بنابراین از پیامدهای نامطلوب همولیز و پلی سیتمی جلوگیری می کند.
لکوسیت ها در C-PRP
وجود گلبول های سفید در آماده سازی PRP بستگی به تجهیزات درمان و طرح آماده سازی دارد.در تجهیزات PRP مبتنی بر پلاسما، گلبول های سفید خون به طور کامل حذف می شوند.با این حال، گلبول های سفید خون به طور قابل توجهی در آماده سازی PRP لایه قهوه ای رسوب گلبول قرمز متمرکز شد.گلبولهای سفید به دلیل مکانیسمهای دفاعی ایمنی و میزبان، تأثیر زیادی بر بیولوژی داخلی شرایط بافتی حاد و مزمن دارند.این ویژگی ها در ادامه بیشتر مورد بحث قرار خواهند گرفت.بنابراین وجود لکوسیت های خاص در C-PRP می تواند اثرات سلولی و بافتی قابل توجهی ایجاد کند.به طور خاص، سیستمهای مختلف لایهای زرد-قهوهای رسوب گلبول قرمز PRP از طرحهای آمادهسازی متفاوتی استفاده میکنند، بنابراین نسبت متفاوتی از نوتروفیلها، لنفوسیتها و مونوسیتها در PRP تولید میشوند.ائوزینوفیل ها و بازوفیل ها را نمی توان در آماده سازی PRP اندازه گیری کرد زیرا غشای سلولی آنها برای مقاومت در برابر نیروهای پردازش گریز از مرکز بسیار شکننده است.
نوتروفیل ها
نوتروفیل ها لکوسیت های ضروری در بسیاری از مسیرهای درمانی هستند.این مسیرها با پروتئینهای ضد میکروبی موجود در پلاکتها ترکیب میشوند تا یک سد متراکم در برابر پاتوژنهای مهاجم تشکیل دهند.وجود نوتروفیل ها با توجه به هدف درمانی C-PRP تعیین می شود.افزایش سطوح التهاب بافتی ممکن است در بیوتراپی PRP مراقبت از زخم مزمن یا در کاربردهایی با هدف رشد یا بهبود استخوان مورد نیاز باشد.نکته مهم، عملکردهای اضافی نوتروفیل در چندین مدل یافت شده است که بر نقش آنها در رگزایی و ترمیم بافت تأکید می کند.با این حال، نوتروفیل ها نیز می توانند اثرات مضری داشته باشند، بنابراین برای برخی از کاربردها مناسب نیستند.ژو و وانگ ثابت کردند که استفاده از PRP غنی از نوتروفیل ها می تواند منجر به افزایش نسبت کلاژن نوع III به کلاژن نوع I شود، در نتیجه فیبروز را تشدید کرده و قدرت تاندون را کاهش می دهد.سایر ویژگیهای مضر با واسطه نوتروفیلها، آزادسازی سیتوکینهای التهابی و متالوپروتئینازهای ماتریکس (MMPs) است که میتواند باعث التهاب و کاتابولیسم در بافتها شود.
لکومونوسیت
در C-PRP، لنفوسیت های T و B تک هسته ای بیش از هر گلبول سفید دیگری متمرکز هستند.آنها ارتباط نزدیکی با ایمنی تطبیقی سیتوتوکسیک سلولی دارند.لنفوسیت ها می توانند واکنش های سلولی را برای مبارزه با عفونت و سازگاری با مهاجمان تحریک کنند.علاوه بر این، سیتوکین های مشتق از لنفوسیت T (اینترفرون γ [IFN-γ] و اینترلوکین-4 (IL-4) قطبش ماکروفاژها را افزایش می دهند. Verassar و همکاران ثابت شده است که لنفوسیت های T معمولی می توانند به طور غیرمستقیم باعث بهبود بافت در مدل موش با تنظیم تمایز مونوسیت ها و ماکروفاژها.
مونوسیت - سلول ترمیم کننده چند توان
با توجه به دستگاه آماده سازی PRP استفاده شده، مونوسیت ها ممکن است در بطری درمان PRP بیرون زده یا وجود نداشته باشند.متأسفانه، عملکرد و توانایی بازسازی آنها به ندرت در ادبیات مورد بحث قرار گرفته است.بنابراین در روش تهیه یا فرمول نهایی به مونوسیت ها توجه کمی می شود.گروه مونوسیتی ناهمگن است که از سلول های پیش ساز در مغز استخوان منشأ می گیرد و از طریق مسیر سلول های بنیادی خونساز بر اساس تحریک ریزمحیط به بافت های محیطی منتقل می شود.در طول هموستاز و التهاب، مونوسیتهای در گردش جریان خون را ترک میکنند و به بافتهای آسیبدیده یا تخریبشده جذب میشوند.آنها می توانند به عنوان ماکروفاژها (M Φ) سلول های موثر یا سلول های پیش ساز عمل کنند.مونوسیتها، ماکروفاژها و سلولهای دندریتیک نشاندهنده سیستم فاگوسیتی تکهستهای (MPS) هستند. یکی از ویژگیهای معمول MPS انعطافپذیری الگوی بیان ژن آن و همپوشانی عملکردی بین این انواع سلول است.در بافتهای دژنره شده، ماکروفاژهای ساکن، فاکتورهای رشد موضعی، سیتوکینهای پیش التهابی، سلولهای آپوپتوز یا نکروزه و محصولات میکروبی، مونوسیتها را برای تمایز به گروههای سلولی MPS آغاز میکنند.فرض کنید وقتی C-PRP حاوی مونوسیتهای با بازده بالا به ریزمحیط محلی بیماری تزریق میشود، مونوسیتها احتمالاً به M Φ متمایز میشوند تا تغییرات عمدهای در سلول ایجاد کنند.
از مونوسیت به M Φ در فرآیند تبدیل، فنوتیپ M Φ خاص.در ده سال گذشته، مدلی توسعه یافته است که M Φ را ادغام می کند. مکانیسم پیچیده فعال سازی به عنوان قطبش دو حالت متضاد توصیف می شود: M Φ فنوتیپ 1 (M Φ 1، فعال سازی کلاسیک) و M Φ فنوتیپ 2 (M Φ). 2، فعال سازی جایگزین).M Φ 1 با ترشح سیتوکین التهابی (IFN-γ) و اکسید نیتریک برای تولید مکانیسم موثر کشتن پاتوژن مشخص می شود.M Φ فنوتیپ همچنین فاکتور رشد اندوتلیال عروقی (VEGF) و فاکتور رشد فیبروبلاست (FGF) را تولید می کند.M Φ فنوتیپ از سلول های ضد التهابی با فاگوسیتوز بالا تشکیل شده است.M Φ 2 اجزای ماتریکس خارج سلولی، رگ زایی و کموکاین ها و اینترلوکین 10 (IL-10) را تولید می کند.علاوه بر دفاع پاتوژن، M Φ همچنین می تواند التهاب را کاهش داده و ترمیم بافت را تقویت کند.قابل توجه است که M Φ 2 به M در شرایط آزمایشگاهی Φ 2a、M Φ 2b و M Φ 2 تقسیم شده است. بستگی به محرک دارد.ترجمه in vivo این زیرگروه ها دشوار است زیرا بافت ممکن است حاوی گروه های M Φ مخلوط باشد.جالب توجه است، بر اساس سیگنال های محیطی محلی و سطوح IL-4، M Φ 1 پیش التهابی را می توان برای ترویج ترمیم M Φ 2 تبدیل کرد. از این داده ها، منطقی است فرض کنیم که غلظت بالایی از مونوسیت ها و آماده سازی M Φ C-PRP وجود دارد. ممکن است به ترمیم بهتر بافت کمک کنند زیرا آنها دارای قابلیت ترمیم بافت ضد التهابی و قابلیت انتقال سیگنال سلولی هستند.
تعریف گیج کننده کسر گلبول های سفید در PRP
وجود گلبول های سفید در بطری های درمان PRP بستگی به دستگاه آماده سازی PRP دارد و ممکن است تفاوت های قابل توجهی داشته باشد.اختلافات زیادی در مورد وجود لکوسیت ها و سهم آنها در محصولات مختلف زیر PRP (مانند PRGF، P-PRP، LP-PRP، LR-PRP، P-PRF و L-PRF) وجود دارد. در یک بررسی اخیر، شش مورد تصادفی کارآزماییهای کنترلشده (سطح شواهد 1) و سه مطالعه تطبیقی آیندهنگر (سطح شواهد 2) شامل 1055 بیمار بودند که نشان میدهد LR-PRP و LP-PRP ایمنی مشابهی داشتند.نویسنده نتیجه گرفت که واکنش نامطلوب PRP ممکن است به طور مستقیم با غلظت گلبول های سفید مرتبط نباشد.در مطالعه دیگری، LR-PRP اینترلوکین التهابی (IL-1) را در OA زانو β، IL-6، IL-8 و IL-17 تغییر نداد.این نتایج این دیدگاه را تأیید می کند که نقش لکوسیت ها در فعالیت بیولوژیکی PRP در داخل بدن ممکن است از تداخل بین پلاکت ها و لکوسیت ها ناشی شود.این فعل و انفعال می تواند بیوسنتز سایر عوامل (مانند لیپوکسیژن) را تقویت کند، که می تواند پسرفت التهاب را خنثی یا تقویت کند.پس از آزاد شدن اولیه مولکول های التهابی (آراشیدونیک اسید، لکوترین و پروستاگلاندین)، لیپوکسیژن A4 از پلاکت های فعال شده آزاد می شود تا از فعال شدن نوتروفیل ها جلوگیری کند.در این محیط است که فنوتیپ M Φ از M Φ 1 به M Φ 2 تغییر می کند. علاوه بر این، شواهد فزاینده ای وجود دارد که سلول های تک هسته ای در گردش می توانند به انواع سلول های غیر فاگوسیتی به دلیل پرتوانی شان تمایز پیدا کنند.
نوع PRP روی کشت MSC تاثیر می گذارد.در مقایسه با نمونههای PRP یا PPP خالص، LR-PRP میتواند با آزادسازی سریعتر و فعالیت بیولوژیکی PGF بهتر، تکثیر قابلتوجهی سلولهای بنیادی مزانشیمی مشتق از مغز استخوان (BMMSCs) را القا کند.همه این ویژگیها برای افزودن مونوسیتها به بطری درمان PRP و تشخیص توانایی تعدیلکننده ایمنی و پتانسیل تمایز آنها مفید است.
تنظیم ایمنی مادرزادی و سازگار PRP
معروف ترین عملکرد فیزیولوژیکی پلاکت ها کنترل خونریزی است.آنها در محل آسیب بافتی و رگ های خونی آسیب دیده تجمع می یابند.این رویدادها ناشی از بیان اینتگرین ها و سلکتین ها هستند که چسبندگی و تجمع پلاکت ها را تحریک می کنند.اندوتلیوم آسیبدیده این فرآیند را تشدید میکند و کلاژن در معرض و سایر پروتئینهای ماتریکس زیر اندوتلیال باعث فعال شدن عمیق پلاکتها میشود.در این موارد نقش مهم برهمکنش فاکتور فون ویلبراند (vWF) و گلیکوپروتئین (GP) به ویژه GP-Ib به اثبات رسیده است.پس از فعال شدن پلاکت، پلاکت α-、 متراکم، لیزوزوم و گرانول های T اگزوسیتوز را تنظیم کرده و محتویات خود را در محیط خارج سلولی آزاد می کنند.
مولکول چسبندگی پلاکت
به منظور درک بهتر نقش PRP در بافتهای التهابی و پلاکتها در پاسخ ایمنی، باید بدانیم که چگونه گیرندههای مختلف سطح پلاکت (اینتگرین) و مولکولهای چسبندگی اتصال (JAM) و تعاملات سلولی میتوانند فرآیندهای حیاتی را در ایمنی ذاتی و تطبیقی آغاز کنند.
اینتگرین ها مولکول های چسبنده سطح سلولی هستند که در انواع مختلف سلول یافت می شوند و به مقدار زیاد روی پلاکت ها بیان می شوند.اینتگرین ها عبارتند از a5b1، a6b1، a2b1 LFA-2، (GPIa/IIa) و aIIbb3 (GPIIb/IIIa).معمولاً در حالت ایستا و میل ترکیبی کم وجود دارند.پس از فعال شدن، آنها به حالت میل پیوند لیگاند بالا می روند.اینتگرین ها عملکردهای متفاوتی روی پلاکت ها دارند و در برهمکنش پلاکت ها با چندین نوع گلبول سفید، سلول های اندوتلیال و ماتریکس خارج سلولی شرکت می کنند.علاوه بر این، کمپلکس GP-Ib-V-IX بر روی غشای پلاکتی بیان می شود و گیرنده اصلی اتصال با فون vWF است.این تعامل واسطه تماس اولیه بین پلاکت ها و ساختارهای زیر اندوتلیال در معرض قرار می گیرد.اینتگرین پلاکتی و کمپلکس GP با فرآیندهای التهابی مختلف مرتبط هستند و نقش مهمی در تشکیل کمپلکس پلاکت - لکوسیت دارند.به طور خاص، اینتگرین aIIbb3 برای تشکیل یک کمپلکس پایدار با ترکیب فیبرینوژن با گیرنده آنتی ژن ماکروفاژ 1 (Mac-1) روی نوتروفیل ها ضروری است.
پلاکتها، نوتروفیلها و سلولهای اندوتلیال عروقی، مولکولهای چسبندگی سلولی خاصی به نام سلکتین را بیان میکنند.در شرایط التهابی، پلاکت ها P-سلکتین و نوتروفیل L-سلکتین را بیان می کنند.پس از فعال شدن پلاکت، P-سلکتین ممکن است به لیگاند PSGL-1 که روی نوتروفیل ها و مونوسیت ها وجود دارد متصل شود.علاوه بر این، اتصال PSGL-1 واکنش آبشاری سیگنال درون سلولی را آغاز می کند، که نوتروفیل ها را از طریق نوتروفیل اینتگرین Mac-1 و آنتی ژن 1 مرتبط با عملکرد لنفوسیت (LFA-1) فعال می کند.Mac-1 فعال شده از طریق فیبرینوژن به GPIb یا GPIIb/IIIa روی پلاکت ها متصل می شود، بنابراین تعامل بین نوتروفیل ها و پلاکت ها را تثبیت می کند.علاوه بر این، LFA-1 فعال شده می تواند با مولکول چسبندگی بین سلولی پلاکت 2 ترکیب شود تا کمپلکس نوتروفیل-پلاکت را بیشتر تثبیت کند تا چسبندگی طولانی مدت با سلول ها را تقویت کند.
پلاکت ها و لکوسیت ها نقش کلیدی در پاسخ های ایمنی ذاتی و سازگار ایفا می کنند
بدن می تواند اجسام خارجی و بافت های آسیب دیده را در بیماری های حاد یا مزمن شناسایی کند تا واکنش آبشاری بهبود زخم و مسیر التهابی را آغاز کند.سیستم ایمنی ذاتی و سازگار از میزبان در برابر عفونت محافظت می کند و گلبول های سفید نقش مهمی در همپوشانی بین این دو سیستم دارند.به طور خاص، مونوسیتها، ماکروفاژها، نوتروفیلها و سلولهای کشنده طبیعی نقش کلیدی در سیستم ذاتی دارند، در حالی که لنفوسیتها و زیرمجموعههای آنها نقشی مشابه در سیستم ایمنی سازگار دارند.
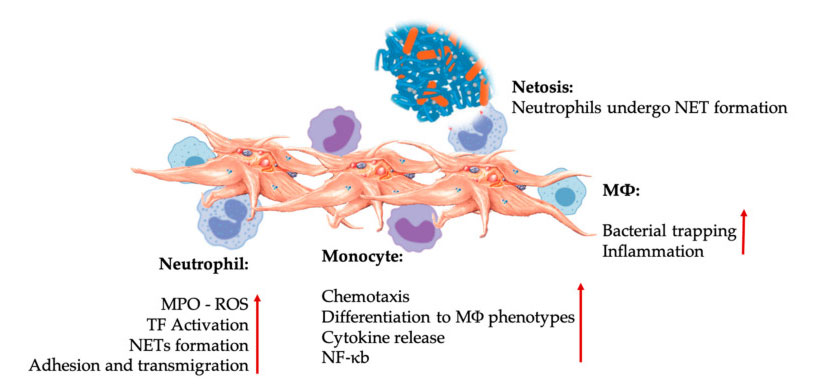
برهمکنش پلاکت ها و لکوسیت ها در فعل و انفعالات سلول های ایمنی ذاتیپلاکتها با نوتروفیلها و مونوسیتها برهمکنش میکنند و در نهایت با M Φ Interact، عملکردهای مؤثر آنها را تنظیم و افزایش میدهند.این فعل و انفعالات پلاکت-لکوسیت از طریق مکانیسم های مختلف از جمله NETosis منجر به التهاب می شود.اختصارات: MPO: میلوپراکسیداز، ROS: گونه های فعال اکسیژن، TF: فاکتور بافتی، NET: تله خارج سلولی نوتروفیل، NF-κ B: فاکتور هسته ای کاپا B، M Φ: ماکروفاژها.
سیستم ایمنی ذاتی
نقش سیستم ایمنی ذاتی شناسایی غیر اختصاصی میکروارگانیسم های مهاجم یا قطعات بافتی و تحریک پاکسازی آنهاست.هنگامی که ساختارهای مولکولی خاصی به نام گیرنده های تشخیص الگوی بیان سطحی (PRRs) با الگوهای مولکولی مرتبط با پاتوژن و الگوهای مولکولی مرتبط با آسیب ترکیب شوند، سیستم ایمنی ذاتی فعال می شود.انواع مختلفی از PRR وجود دارد، از جمله گیرنده Toll مانند (TLR) و گیرنده RIG-1 (RLR).این گیرنده ها می توانند فاکتور رونویسی اصلی کاپا B (NF-κ B) را فعال کنند و همچنین جنبه های متعدد پاسخ ایمنی ذاتی و تطبیقی را تنظیم می کند.جالب توجه است که پلاکت ها همچنین انواعی از مولکول های گیرنده تنظیم کننده ایمنی را بر روی سطح و سیتوپلاسم خود بیان می کنند، مانند P-selectin، لیگاند CD40 پروتئین گذرنده (CD40L)، سیتوکین ها (مانند IL-1 β، TGF-β) و TLR اختصاصی پلاکتی. بنابراین، پلاکت ها می توانند با سلول های ایمنی مختلف تعامل داشته باشند.
تعامل پلاکت-سلول سفید در ایمنی ذاتی
هنگامی که پلاکت ها وارد جریان خون یا بافت می شوند یا به آن حمله می کنند، پلاکت ها یکی از سلول هایی هستند که ابتدا آسیب اندوتلیال و پاتوژن های میکروبی را تشخیص می دهند.تجمع پلاکتی و ترویج آزادسازی آگونیست های پلاکتی ADP، ترومبین و vWF، در نتیجه فعال شدن پلاکت و بیان گیرنده های کموکاین پلاکتی C، CC، CXC و CX3C، در نتیجه باعث ایجاد پلاکت ها در محل آلوده یا آسیب می شود.
سیستم ایمنی ذاتی از نظر ژنتیکی برای شناسایی مهاجمانی مانند ویروس ها، باکتری ها، انگل ها و سموم یا زخم ها و زخم های بافتی از پیش تعیین شده است.این یک سیستم غیر اختصاصی است، زیرا هر عامل بیماری زا به عنوان خارجی یا غیر خود شناسایی می شود و به سرعت شناسایی می شود.سیستم ایمنی ذاتی به مجموعه ای از پروتئین ها و فاگوسیت ها متکی است که ویژگی های به خوبی حفظ شده پاتوژن ها را تشخیص می دهند و به سرعت پاسخ ایمنی را برای کمک به از بین بردن مهاجمان فعال می کنند، حتی اگر میزبان قبلاً هرگز در معرض پاتوژن های خاصی قرار نگرفته باشد.
نوتروفیل ها، مونوسیت ها و سلول های دندریتیک شایع ترین سلول های ایمنی ذاتی در خون هستند.استخدام آنها برای یک پاسخ ایمنی اولیه کافی ضروری است.هنگامی که PRP در پزشکی احیا کننده استفاده می شود، تعامل پلاکت-سلول سفید التهاب، بهبود زخم و ترمیم بافت را تنظیم می کند.TLR-4 روی پلاکتها برهمکنش پلاکت-نوتروفیل را تحریک میکند، که با تنظیم آزادسازی گونههای فعال اکسیژن (ROS) و میلوپراکسیداز (MPO) از نوتروفیلها، به اصطلاح انفجار اکسیداتیو لکوسیتی را تنظیم میکند.علاوه بر این، تعامل بین پلاکت-نوتروفیل و دگرانولاسیون نوتروفیل منجر به تشکیل تله های نوتروفیل-خارج سلولی (NETs) می شود.NET ها از هسته نوتروفیل و سایر محتویات داخل سلولی نوتروفیل تشکیل شده اند که می توانند باکتری ها را گرفته و از طریق NETosis از بین ببرند.تشکیل NET ها یک مکانیسم ضروری کشتن نوتروفیل ها است.
پس از فعال شدن پلاکت ها، مونوسیت ها می توانند به بافت های بیمار و دژنراتیو مهاجرت کنند، جایی که فعالیت های چسبندگی را انجام می دهند و مولکول های التهابی ترشح می کنند که ممکن است کموتاکسی و خواص پروتئولیتیک را تغییر دهند.علاوه بر این، پلاکت ها می توانند فعال شدن مونوسیت NF-κ B را برای تنظیم عملکرد مؤثر مونوسیت ها، که واسطه کلیدی پاسخ التهابی و فعال سازی و تمایز سلول های ایمنی است، القا کنند.پلاکت ها بیشتر باعث افزایش انفجار اکسیداتیو درون زا مونوسیت ها برای ترویج تخریب پاتوژن های فاگوسیتی می شوند.انتشار MPO با برهمکنش مستقیم بین پلاکت-مونوسیت CD40L-MAC-1 انجام می شود.جالب توجه است، هنگامی که P-سلکتین پلاکت ها را تحت شرایط بافت التهابی حاد و مزمن فعال می کند، کموکاین های مشتق از پلاکت PF4، RANTES، IL-1 β و CXCL-12 می توانند از آپوپتوز خود به خودی مونوسیت ها جلوگیری کنند، اما تمایز آنها را به ماکروفاژها افزایش می دهند.
سیستم ایمنی تطبیقی
پس از اینکه سیستم ایمنی ذاتی غیر اختصاصی آسیب میکروبی یا بافتی را تشخیص داد، سیستم ایمنی تطبیقی خاص مسئولیت را بر عهده خواهد گرفت.سیستم های تطبیقی شامل لنفوسیت های B متصل شونده به آنتی ژن (سلول های B) و لنفوسیت های T معمولی (Treg) هستند که پاکسازی پاتوژن ها را هماهنگ می کنند.سلولهای T را میتوان تقریباً به سلولهای T کمکی (سلولهای Th) و سلولهای T سیتوتوکسیک (سلولهای Tc که به عنوان سلولهای T کشنده نیز شناخته میشوند) تقسیم کرد.سلول های Th بیشتر به سلول های Th1، Th2 و Th17 تقسیم می شوند که عملکردهای کلیدی در التهاب دارند.سلولهای Th میتوانند سیتوکینهای پیشالتهابی (مانند IFN-γ، TNF-β) و چندین اینترلوکین (مانند IL-17) ترشح کنند. این سلولها بهویژه در پیشگیری از ویروسهای داخل سلولی و عفونت باکتریایی مؤثر هستند. سلولهای Th تکثیر و تمایز سلولهای درگیر را تحریک میکنند. پاسخ ایمنی سلول های Tc سلول های موثری هستند که می توانند میکروارگانیسم ها و سلول های هدفمند درون سلولی و خارج سلولی را از بین ببرند.
جالب توجه است که سلولهای Th2 IL-4 تولید میکنند و بر قطبش M Φ، M Φ بازآفرینی هدایتشده M Φ 2 فنوتیپ تأثیر میگذارند، در حالی که IFN-γ M Φ به فنوتیپ M Φ1 التهابی تغییر میکند، که به دوز و زمان سیتوکینها بستگی دارد.پس از فعال شدن IL-4، M Φ2 سلول های Treg را وادار می کند تا به سلول های Th2 متمایز شوند و سپس IL-4 اضافی (حلقه بازخورد مثبت) تولید می کند.سلولهای Th M Φ را تبدیل میکنند. فنوتیپ در پاسخ به عوامل بیولوژیکی منشأ بافتی به فنوتیپ احیاکننده هدایت میشود.این مکانیسم مبتنی بر شواهدی است که نشان میدهد سلولهای Th نقش مهمی در کنترل التهاب و ترمیم بافت دارند.
تعامل پلاکت-سلول سفید در ایمنی تطبیقی
سیستم ایمنی تطبیقی از گیرنده های اختصاصی آنتی ژن استفاده می کند و پاتوژن هایی را که قبلاً با آن مواجه شده اند به خاطر می آورد و هنگامی که متعاقباً با میزبان روبرو می شود آنها را از بین می برد.با این حال، این پاسخ های ایمنی تطبیقی به کندی توسعه یافتند.کونیاس و همکاراناین نشان می دهد که جزء پلاکتی به درک خطر و ترمیم بافت کمک می کند و تعامل بین پلاکت ها و لکوسیت ها باعث فعال شدن پاسخ ایمنی تطبیقی می شود.
در طول پاسخ ایمنی تطبیقی، پلاکتها پاسخهای مونوسیت و ماکروفاژ را از طریق بلوغ سلولهای DC و NK ارتقا میدهند که منجر به پاسخهای خاص سلولهای T و B میشود.بنابراین، اجزای گرانول پلاکتی با بیان CD40L، مولکولی که برای تنظیم پاسخ ایمنی تطبیقی ضروری است، مستقیماً بر ایمنی تطبیقی تأثیر میگذارند.پلاکت ها از طریق CD40L نه تنها در ارائه آنتی ژن نقش دارند، بلکه بر واکنش سلول های T نیز تأثیر می گذارند.لیو و همکارانمشخص شد که پلاکت ها پاسخ سلول های CD4 T را به روشی پیچیده تنظیم می کنند.این تنظیم افتراقی زیرمجموعههای سلولهای CD4 T به این معنی است که پلاکتها سلولهای CD4 T را برای پاسخ به محرکهای التهابی ارتقا میدهند، بنابراین پاسخهای پیشالتهابی و ضد التهابی قوی ایجاد میکنند.
پلاکت ها همچنین پاسخ تطبیقی با واسطه سلول های B به پاتوژن های میکروبی را تنظیم می کنند.به خوبی شناخته شده است که CD40L روی سلولهای CD4 T فعال، CD40 سلولهای B را تحریک میکند و دومین سیگنال مورد نیاز برای فعالسازی لنفوسیت B وابسته به سلول T، تبدیل آلوتیپ بعدی، و تمایز و تکثیر سلولهای B را فراهم میکند.به طور کلی، نتایج به وضوح عملکردهای مختلف پلاکتها را در ایمنی تطبیقی نشان میدهند، که نشان میدهد پلاکتها تعامل بین سلولهای T و سلولهای B را از طریق CD40-CD40L به هم متصل میکنند، بنابراین پاسخ سلولهای B وابسته به سلول T را افزایش میدهند.علاوه بر این، پلاکتها غنی از گیرندههای سطح سلولی هستند که میتوانند باعث فعال شدن پلاکتها شوند و تعداد زیادی مولکول فعال التهابی و بیولوژیکی ذخیره شده در ذرات پلاکتی مختلف را آزاد کنند، بنابراین بر پاسخ ایمنی ذاتی و سازگار تأثیر میگذارند.
نقش گسترده سروتونین مشتق از پلاکت در PRP
سروتونین (5-هیدروکسی تریپتامین، 5-HT) نقش کلیدی روشنی در سیستم عصبی مرکزی (CNS)، از جمله تحمل درد دارد.تخمین زده می شود که بیشتر 5-HT انسان در دستگاه گوارش و سپس از طریق گردش خون تولید می شود، جایی که از طریق ناقل بازجذب سروتونین توسط پلاکت ها جذب شده و در ذرات متراکم با غلظت بالا (65 میلی مول در لیتر) ذخیره می شود.5-HT یک انتقال دهنده عصبی و هورمون شناخته شده است که به تنظیم فرآیندهای عصبی روانشناختی مختلف در CNS (5-HT مرکزی) کمک می کند.با این حال، بیشتر 5-HT خارج از CNS (5-HT محیطی) وجود دارد، و در تنظیم عملکردهای بیولوژیکی سیستمیک و سلولی سیستمهای اندام متعدد، از جمله سیستمهای عملکردی قلبی عروقی، ریه، دستگاه گوارش، ادراری-تناسلی و پلاکتی نقش دارد.5-HT دارای متابولیسم وابسته به غلظت بر روی انواع سلول ها از جمله سلول های چربی، سلول های اپیتلیال و گلبول های سفید است.5-HT محیطی همچنین یک تعدیل کننده ایمنی قوی است که می تواند التهاب را تحریک یا مهار کند و از طریق گیرنده 5-HT خاص خود (5HTR) بر سلول های ایمنی مختلف تأثیر بگذارد.
مکانیسم پاراکرین و اتوکرین HT
فعالیت 5-HT توسط تعامل آن با 5HTR ها انجام می شود، که یک ابرخانواده با هفت عضو (5-HT 1-7) و حداقل 14 زیرگروه گیرنده مختلف، از جمله عضو اخیراً کشف شده 5-HT 7، محیطی و عملکرد در مدیریت درددر فرآیند دگرانولاسیون پلاکتی، پلاکتهای فعال شده تعداد زیادی 5-HT مشتق از پلاکت ترشح میکنند که میتواند انقباض عروقی را تقویت کرده و فعال شدن پلاکتها و لنفوسیتهای مجاور را از طریق بیان 5-HTR روی سلولهای اندوتلیال، سلولهای ماهیچه صاف و تحریک کند. سلول های ایمنیپاکالا و همکاراناثر میتوزی 5-HT بر سلول های اندوتلیال عروقی مورد مطالعه قرار گرفت و پتانسیل ارتقاء رشد رگ های خونی آسیب دیده با تحریک رگ زایی تعیین شد.نحوه تنظیم این فرآیندها به طور کامل مشخص نیست، اما ممکن است شامل مسیرهای سیگنال دو طرفه افتراقی در ریزمدار بافت برای تنظیم عملکرد سلولهای اندوتلیال عروقی و سلولهای ماهیچه صاف، فیبروبلاستها و سلولهای ایمنی از طریق گیرندههای خاص 5-HT روی این سلولها باشد. .عملکرد اتوکرین پلاکت 5-HT پس از فعال سازی پلاکتی شرح داده شده است [REF].انتشار 5-HT باعث افزایش فعال شدن پلاکت ها و جذب پلاکت های در گردش می شود که منجر به فعال شدن واکنش های آبشاری سیگنال و عوامل بالادستی می شود که از واکنش پلاکتی حمایت می کنند.
اثر 5-HT تعدیل کننده ایمنی
شواهد بیشتر و بیشتر نشان می دهد که سروتونین می تواند در 5HTR مختلف به عنوان تعدیل کننده ایمنی نقش داشته باشد.با توجه به 5HTR بیان شده در لکوسیت های مختلف درگیر در واکنش التهابی، 5-HT مشتق از پلاکت به عنوان یک تنظیم کننده ایمنی در هر دو سیستم ایمنی ذاتی و سازگار عمل می کند.5-HT میتواند تکثیر Treg را تحریک کرده و عملکرد سلولهای B، سلولهای کشنده طبیعی و نوتروفیلها را با بهکارگیری DC و مونوسیتها در محل التهاب تنظیم کند.مطالعات اخیر نشان داده است که 5-HT مشتق از پلاکت می تواند عملکرد سلول های ایمنی را تحت شرایط خاص تنظیم کند.بنابراین، با استفاده از C-PRP، غلظت پلاکتی بیشتر از 1 × 10 6/μL می تواند به طور قابل توجهی به انتقال غلظت 5-HT مشتق شده از پلاکت های بزرگ به بافت کمک کند.در ریزمحیطی که با اجزای التهابی مشخص میشود، PRP میتواند با چندین سلول ایمنی که نقش کلیدی در این آسیبشناسی دارند، تعامل داشته باشد، که ممکن است بر نتایج بالینی تأثیر بگذارد.
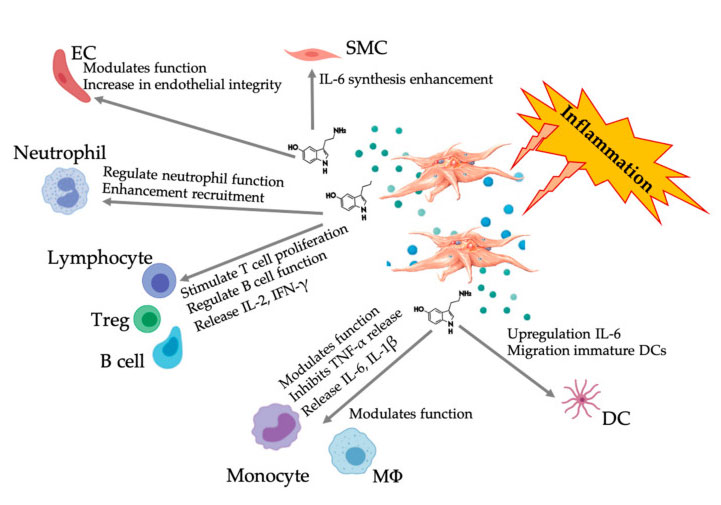
شکلی که پاسخ چندوجهی 5-HT را پس از فعال شدن پلاکت های التهابی PRP نشان می دهد.پس از فعال شدن پلاکت ها، پلاکت ها گرانول های خود را آزاد می کنند، از جمله 5-HT در گرانول های متراکم، که طیف وسیعی از اثرات افتراقی بر روی سلول های مختلف ایمنی، سلول های اندوتلیال و سلول های ماهیچه صاف دارد.اختصارات: SMC: سلول های ماهیچه صاف، EC: سلول های اندوتلیال، Treg: لنفوسیت های T معمولی، M Φ: ماکروفاژها، DC: سلول های دندریتیک، IL: اینترلوکین، IFN-γ: اینترفرون γ. اصلاح شده و اقتباس شده از Everts و همکاران.و هال و همکاران
اثر ضد درد PRP
پلاکت های فعال بسیاری از واسطه های پیش التهابی و ضد التهابی را آزاد می کنند که نه تنها می توانند باعث درد شوند، بلکه التهاب و درد را نیز کاهش می دهند.پس از اعمال، دینامیک پلاکتی معمولی PRP، ریزمحیط را قبل از ترمیم و بازسازی بافت از طریق انواع مسیرهای پیچیده مرتبط با آنابولیسم و کاتابولیسم، تکثیر سلولی، تمایز و تنظیم سلول های بنیادی تغییر می دهد.این ویژگیهای PRP منجر به کاربرد PRP در شرایط پاتولوژیک بالینی مختلف میشود که معمولاً با درد مزمن همراه است (مانند آسیبهای ورزشی، بیماریهای ارتوپدی، بیماری ستون فقرات و زخم مزمن پیچیده)، اگرچه مکانیسم دقیق آن به طور کامل مشخص نشده است.
در سال 2008، Evertz و همکاران.این اولین کارآزمایی تصادفیسازی و کنترلشده است که اثر ضددردی آمادهسازی PRP را گزارش میکند که از لایه قهوهای سرعت رسوب گلبولهای قرمز اتولوگ تهیه شده و پس از جراحی شانه با ترومبین اتولوگ فعال میشود.آنها به کاهش قابل توجه نمرات مقیاس آنالوگ بصری، استفاده از مسکن های مبتنی بر مواد افیونی و توانبخشی موفق بعد از عمل اشاره کردند.قابل توجه است که آنها اثر ضد درد پلاکت های فعال شده را منعکس می کنند و در مورد مکانیسم انتشار 5-HT پلاکت ها حدس می زنند.به طور خلاصه، پلاکت ها در پی آر پی تازه آماده شده غیرفعال هستند.پس از فعال شدن پلاکت ها به طور مستقیم یا غیرمستقیم (فاکتور بافتی)، پلاکت ها تغییر شکل می دهند و به اندازه کافی کاذب تولید می کنند که باعث تجمع پلاکتی شود.سپس ذرات α- و متراکم درون سلولی را آزاد می کنند.بافت تحت درمان با PRP فعال شده توسط PGF، سیتوکین ها و سایر لیزوزوم های پلاکتی مورد تهاجم قرار می گیرد.به طور خاص، هنگامی که ذرات متراکم محتویات خود را آزاد می کنند، مقدار زیادی 5-HT آزاد می کنند که درد را تنظیم می کند.در C-PRP غلظت پلاکت 5 تا 7 برابر بیشتر از خون محیطی است.بنابراین، انتشار 5-HT از پلاکت ها نجومی است.جالب توجه است که Sprott و همکاران.این گزارش مشاهده کرد که درد به طور قابل توجهی پس از طب سوزنی و moxibustion کاهش یافت، غلظت 5-HT مشتق از پلاکت به طور قابل توجهی کاهش یافت و سپس سطح 5-HT پلاسما افزایش یافت.
در محیطی، پلاکت ها، ماست سل ها و سلول های اندوتلیال 5-HT درون زا را در طی آسیب بافتی یا ترومای جراحی آزاد می کنند.جالب توجه است که انواعی از گیرندههای 5-HT از نورونها در ناحیه محیطی شناسایی شدند که تأیید میکنند که 5-HT میتواند با انتقال درد در ناحیه محیطی تداخل ایجاد کند.این مطالعات نشان می دهد که 5-HT می تواند بر انتقال درد بافت های محیطی از طریق گیرنده های 5-HT1، 5-HT2، 5-HT3، 5-HT4 و 5-HT7 تأثیر بگذارد.
سیستم 5-HT نشان دهنده یک سیستم قدرتمند است که می تواند باعث کاهش و افزایش درجه درد پس از تحریک مضر شود.تنظیم مرکزی و محیطی سیگنال های درد و تغییرات در سیستم 5-HT در بیماران مبتلا به درد مزمن گزارش شده است.در سالهای اخیر، تعداد زیادی از مطالعات بر روی نقش 5-HT و گیرندههای مربوط به آن در پردازش و تنظیم اطلاعات مضر متمرکز شدهاند که منجر به تولید داروهایی مانند مهارکنندههای انتخابی بازجذب سروتونین (SSRI) شده است.این دارو پس از آزادسازی سروتونین از بازجذب سروتونین به نورون های پیش سیناپسی جلوگیری می کند.این بر مدت زمان و شدت ارتباط سروتونین تأثیر می گذارد و یک درمان جایگزین برای دردهای مزمن است.تحقیقات بالینی بیشتری برای درک واضح مکانیسم مولکولی تنظیم درد 5-HT مشتق از PRP در بیماری های مزمن و دژنراتیو مورد نیاز است.
سایر داده ها برای حل اثر ضد درد بالقوه PRP را می توان پس از آزمایش مدل حیوانی ضد درد به دست آورد.نتیجهگیریهای آماری مقایسهای در این مدلها چالش برانگیز هستند، زیرا این مطالعات دارای متغیرهای بسیار زیادی هستند.با این وجود، برخی از مطالعات بالینی به اثرات درد و ضد درد PRP پرداخته اند.چندین مطالعه نشان داده است که بیمارانی که برای تاندونوز یا پارگی روتاتور کاف درمان میشوند، تسکین درد کمی دارند.در مقابل، چندین مطالعه دیگر نشان دادهاند که PRP میتواند درد بیماران مبتلا به دژنراسیون تاندون، OA، فاشیای کف پا و سایر بیماریهای پا و مچ پا را کاهش دهد یا حتی از بین ببرد.غلظت نهایی پلاکت و ترکیب سلولی بیولوژیکی به عنوان ویژگی های کلیدی PRP شناسایی شده است که به مشاهده اثر ضد درد ثابت پس از استفاده از PRP کمک می کند.سایر متغیرها شامل روش تحویل PRP، فناوری کاربرد، پروتکل فعال سازی پلاکتی، سطح فعالیت بیولوژیکی PGF و سیتوکین های آزاد شده، نوع بافت کاربرد PRP و نوع آسیب می باشد.
قابل توجه است که کوفلر پتانسیل PRP را در کاهش درد در بیماران مبتلا به درد نوروپاتیک مزمن خفیف تا شدید، ثانویه به عصب غیر بازسازی کننده آسیب دیده، حل کرد.هدف از این مطالعه بررسی این موضوع است که آیا درد نوروپاتیک می تواند به دلیل PRP که باعث بازسازی آکسون و عصب دهی مجدد عصب هدف می شود کاهش یابد یا فروکش کند.با کمال تعجب، در بین بیمارانی که تحت درمان قرار می گیرند، درد نوروپاتیک هنوز حداقل شش سال پس از جراحی از بین می رود یا کاهش می یابد.علاوه بر این، همه بیماران ظرف سه هفته پس از اعمال PRP شروع به تسکین درد کردند.
اخیراً اثرات ضددردی PRP مشابهی در زمینه مراقبت از زخم و پوست پس از عمل مشاهده شده است.جالب توجه است، نویسندگان جنبه های فیزیولوژیکی درد زخم مرتبط با آسیب عروقی و هیپوکسی بافت پوست را گزارش کردند.آنها همچنین در مورد اهمیت رگزایی در بهینه سازی اکسیژن رسانی و تحویل مواد مغذی بحث کردند.مطالعه آنها نشان داد که در مقایسه با گروه کنترل، بیمارانی که درمان PRP را دریافت کردند، درد کمتری داشتند و به طور قابل توجهی رگزایی را افزایش دادند.در نهایت، جوهال و همکارانش یک بررسی سیستماتیک و متاآنالیز انجام دادند و به این نتیجه رسیدند که PRP می تواند درد پس از استفاده از PRP را در اندیکاسیون های ارتوپدی، به ویژه در بیمارانی که درمان اپی کندیلیت خارجی و OA زانو دریافت می کنند، کاهش دهد.متأسفانه، این مطالعه اثرات گلبولهای سفید، غلظت پلاکت یا استفاده از فعالکنندههای پلاکت خارجی را مشخص نکرد، زیرا این متغیرها بر اثربخشی کلی PRP تأثیر میگذارند.غلظت پلاکت PRP بهینه برای حداکثر تسکین درد نامشخص است.در مدل تاندونوز موش، غلظت پلاکت 1.0 × 10 6 / μ در L بود، درد را می توان به طور کامل تسکین داد، در حالی که تسکین درد ناشی از PRP با نیمی از غلظت پلاکتی به طور قابل توجهی کاهش می یابد.بنابراین، ما مطالعات بالینی بیشتری را برای بررسی اثرات ضد درد آمادهسازیهای مختلف PRP تشویق میکنیم.
پی آر پی و اثر رگزایی
آماده سازی C-PRP در پزشکی احیا کننده دقیق امکان تحویل بیومولکول های آزاد شده توسط غلظت های بالای پلاکت های فعال شده در محل های بافت هدف را فراهم می کند.بنابراین، انواع واکنشهای آبشاری آغاز شدهاند که به تنظیم سیستم ایمنی در محل، فرآیند التهابی و رگزایی برای ارتقای بهبود و ترمیم بافت کمک میکنند.
آنژیوژنز یک فرآیند چند مرحله ای پویا است که شامل جوانه زنی و ریزرگ های بافتی از عروق خونی از قبل موجود است.رگ زایی به دلیل مکانیسم های بیولوژیکی متنوعی از جمله مهاجرت سلول های اندوتلیال، تکثیر، تمایز و تقسیم پیشرفت کرده است.این فرآیندهای سلولی پیش نیازی برای تشکیل عروق خونی جدید هستند.آنها برای رشد رگ های خونی موجود برای بازگرداندن جریان خون و حمایت از فعالیت متابولیک بالای ترمیم بافت و بازسازی بافت ضروری هستند.این رگهای خونی جدید امکان تحویل اکسیژن و مواد مغذی و حذف محصولات جانبی از بافتهای تحت درمان را فراهم میکنند.
فعالیت رگ زایی با تحریک فاکتور رگ زایی VEGF و عوامل ضد رگ زایی (مانند آنژیواستاتین و ترومبوسپوندین-1 [TSP-1]) تنظیم می شود.در ریزمحیط بیمار و تخریب شده (از جمله کشش کم اکسیژن، pH پایین و سطح اسید لاکتیک بالا)، عوامل رگ زایی موضعی فعالیت رگ زایی را بازیابی می کنند.
چندین محیط محلول در پلاکت، مانند پایه FGF و TGF-β و VEGF می توانند سلول های اندوتلیال را برای تولید رگ های خونی جدید تحریک کنند.Landsdown و Fortier نتایج مختلف مربوط به ترکیب PRP، از جمله منابع درون پلاکتی بسیاری از تنظیم کننده های رگ زایی را گزارش کردند.علاوه بر این، آنها به این نتیجه رسیدند که افزایش رگزایی به بهبود بیماری MSK در مناطقی با عروق ضعیف، مانند پارگی مینیسک، آسیب تاندون و سایر مناطق با عروق ضعیف کمک می کند.
تقویت و خواص ضد رگ زایی پلاکتی
در چند دهه گذشته، مطالعات منتشر شده ثابت کرده اند که پلاکت ها نقش کلیدی در هموستاز اولیه، تشکیل لخته، فاکتور رشد و آزادسازی سیتوکین و تنظیم رگ زایی به عنوان بخشی از فرآیند ترمیم بافت دارند.به طور متناقض، PRP α- گرانول ها حاوی زرادخانه ای از فاکتورهای رشد پیش رگ زایی، پروتئین های ضد رگ زایی و سیتوکین ها (مانند PF4، مهارکننده فعال کننده پلاسمینوژن-1 و TSP-1) هستند و انتشار عوامل خاصی را هدف قرار می دهند که نقش دارند. .نقش در رگزاییبنابراین، نقش PRP در کنترل تنظیم رگ زایی ممکن است با فعال شدن گیرنده های سطح سلولی خاص، TGF-β شروع کننده واکنش های پیش رگ زایی و ضد رگ زایی تعریف شود.توانایی پلاکت ها در ورزش مسیر رگ زایی در رگ زایی پاتولوژیک و رگ زایی تومور تایید شده است.
فاکتور رشد رگ زایی مشتق از پلاکت و فاکتور رشد ضد رگ زایی، برگرفته از مولکول های α- و متراکم و چسبنده.مهمتر از همه، به طور کلی پذیرفته شده است که اثر کلی پلاکت ها بر رگ زایی، پیش رگ زایی و تحریک کننده است.انتظار می رود که درمان با پی آر پی القای رگ زایی را کنترل کند، که به اثر درمانی بسیاری از بیماری ها مانند بهبود زخم و ترمیم بافت کمک می کند.تجویز PRP، به ویژه تجویز PGF با غلظت بالا و سایر سایتوکاینهای پلاکتی، میتواند باعث رگزایی، رگزایی و شریانزایی شود، زیرا فاکتور 1a مشتق از سلول استرومایی به گیرنده CXCR4 روی سلولهای پیش ساز اندوتلیال متصل میشود.بیل و همکارانپیشنهاد میشود که PRP باعث افزایش نئوواسکولاریزاسیون ایسکمیک میشود که ممکن است به دلیل تحریک رگزایی، رگزایی و شریانزایی باشد.در مدل آزمایشگاهی آنها، تکثیر سلول های اندوتلیال و تشکیل مویرگی توسط تعداد زیادی از PDG های مختلف القا شد که VEGF محرک اصلی رگ زایی بود.یکی دیگر از عوامل مهم و ضروری برای بازیابی مسیر رگزایی، هم افزایی بین چند PGF است.ریچاردسون و همکارانثابت شد که فعالیت هم افزایی فاکتور رگ زایی فاکتور رشد مشتق از پلاکت-bb (PDGF-BB) و VEGF منجر به تشکیل سریع شبکه عروقی بالغ در مقایسه با فعالیت فاکتور رشد فردی شد.اثر ترکیبی این عوامل اخیراً در یک مطالعه بر روی افزایش گردش خون جانبی مغزی در موشهای مبتلا به هیپوپرفیوژن طولانی مدت تأیید شد.
مهمتر از همه، یک مطالعه آزمایشگاهی، اثر تکثیر سلولهای اندوتلیال ورید ناف انسانی و غلظتهای مختلف پلاکتی را بر انتخاب دستگاه آمادهسازی PRP و استراتژی دوز پلاکتی اندازهگیری کرد و نتایج نشان داد که دوز بهینه پلاکت 1.5×106 پلاکت/μ بود. 50. برای ترویج رگ زایی.غلظت بیش از حد پلاکت ممکن است روند رگزایی را مهار کند، بنابراین اثر ضعیف است.
پیری سلولی، پیری و PRP
پیری سلولی می تواند توسط محرک های مختلف القا شود.این فرآیندی است که در آن سلولها تقسیم را متوقف میکنند و برای جلوگیری از رشد نامحدود سلولهای آسیبدیده، که نقش مهمی در پیشگیری از سرطان دارد، تغییرات فنوتیپی منحصربهفردی را تجربه میکنند.در فرآیند پیری فیزیولوژیکی، پیری تکثیر سلولی باعث پیری سلولی میشود و توانایی بازسازی سلولهای بنیادی مزانشیمی کاهش مییابد.
اثرات پیری و پیری سلولی
در داخل بدن، بسیاری از انواع سلول ها پیر می شوند و در بافت های مختلف در طول پیری تجمع می یابند، که در میان آنها تعداد زیادی سلول پیر وجود دارد.به نظر می رسد با افزایش سن، آسیب سیستم ایمنی، آسیب بافتی یا عوامل مرتبط با استرس، تجمع سلول های پیر افزایش می یابد.مکانیسم پیری سلولی به عنوان عامل بیماریزای بیماریهای مرتبط با افزایش سن، مانند استئوآرتریت، پوکی استخوان و دژنراسیون دیسک بین مهرهای شناخته شده است.انواع محرک ها پیری سلول را تشدید می کند.در پاسخ، فنوتیپ ترشحی مرتبط با پیری (SASP) غلظت بالایی از سلول های پروتئینی و سیتوکین ها را ترشح می کند.این فنوتیپ خاص مربوط به سلول های پیر است که در آن سطوح بالایی از سایتوکین های التهابی (مانند IL-1، IL-6، IL-8)، فاکتورهای رشد (مانند TGF-β، HGF، VEGF، PDGF)، ترشح می کنند. MMP و کاتپسین.در مقایسه با افراد جوان، ثابت شده است که SAPS با افزایش سن افزایش مییابد، زیرا فرآیند حالت پایدار از بین میرود و منجر به پیری سلول و کاهش توانایی بازسازی میشود.به طور خاص، در بیماری های مفصلی و بیماری های عضلانی اسکلتی.در این راستا، پیری ایمنی به عنوان یک تغییر قابل توجه در طیف ترشح سلول های ایمنی در نظر گرفته می شود، که نشان می دهد غلظت TNF-a، IL-6 و/یا Il-1b افزایش می یابد و منجر به التهاب مزمن با درجه پایین می شود.شایان ذکر است که اختلال عملکرد سلول های بنیادی به مکانیسم های مستقل غیر سلولی مانند سلول های پیری، به ویژه تولید عوامل پیش التهابی و ضد بازسازی از طریق SASP نیز مرتبط است.
در مقابل، SASP همچنین می تواند انعطاف پذیری سلول و برنامه ریزی مجدد سلول های مجاور را تحریک کند.علاوه بر این، SASP میتواند ارتباط با واسطههای ایمنی مختلف را سازماندهی کند و سلولهای ایمنی را برای ترویج پاکسازی سلولهای پیری فعال کند.درک نقش و عملکرد سلول های پیر به بهبود و بازسازی بافت عضلات MSK و زخم های مزمن کمک می کند.
قابل توجه است که Ritcka و همکاران.یک مطالعه گسترده انجام شد و نقش اصلی و مفید SASP در ارتقاء شکل پذیری سلولی و بازسازی بافت کشف شد و مفهوم تحویل درمانی گذرا سلول های پیر معرفی شد.آنها با احتیاط اشاره کردند که پیری عمدتاً یک فرآیند مفید و احیاکننده است.
پیری سلولی و پتانسیل PRP
با کاهش تعداد سلول های بنیادی، افزایش سن بر عملکرد سلول های بنیادی تأثیر می گذارد.به طور مشابه، در انسان، ویژگی های سلول های بنیادی (مانند خشکی، تکثیر و تمایز) نیز با افزایش سن کاهش می یابد.وانگ و نیرمالا گزارش دادند که افزایش سن ویژگیهای سلولهای بنیادی سلولهای تاندون و تعداد گیرندههای فاکتور رشد را کاهش میدهد.یک مطالعه حیوانی نشان داد که غلظت PDGF در اسب های جوان بالا بود.آنها به این نتیجه رسیدند که افزایش تعداد گیرنده های GF و تعداد GF در افراد جوان ممکن است پاسخ سلولی بهتری به درمان PRP نسبت به افراد مسن در افراد جوان داشته باشد.این یافتهها نشان میدهد که چرا درمان PRP ممکن است در بیماران مسن با سلولهای بنیادی کمتر و «کیفیت پایین» کمتر مؤثر یا حتی بیاثر باشد.ثابت شده است که روند پیری غضروف های پیر معکوس شده و دوره استراحت کندروسیت ها پس از تزریق PRP افزایش می یابد.جیا و همکارانبرای مطالعه فیبروبلاستهای پوستی موش در شرایط آزمایشگاهی، با و بدون درمان PRP، برای روشن شدن مکانیسم مقابله با PGF در این مدل استفاده میشود.گروه PRP اثر مستقیمی بر ماتریکس خارج سلولی، افزایش کلاژن نوع I و کاهش سنتز متالوپروتئینازها نشان داد که نشان میدهد PRP میتواند با پیری سلولی و همچنین در بیماری دژنراتیو MSK مقابله کند.
در مطالعه دیگری، از PRP برای جمع آوری سلول های بنیادی مغز استخوان سالخورده از موش های مسن استفاده شد.مشخص شده است که پی آر پی می تواند انواع مختلفی از عملکردهای سلول های بنیادی مانند تکثیر سلولی و تشکیل کلنی را پس از پیری بازیابی کند و نشانگرهای مربوط به پیری سلول را بازسازی کند.
اخیراً، اوبرلور و همکارانش نقش پیری سلولی را در تضعیف بازسازی عضلات مورد مطالعه قرار دادند و PRP و پلاسمای ضعیف پلاکتی (PPP) را به عنوان گزینههای درمانی بیولوژیکی برای ترمیم عضلات اسکلتی ارزیابی کردند.آنها تصور کردند که درمان PRP یا PPP برای ترمیم عضلات اسکلتی بر اساس عوامل بیولوژیکی سفارشی شده برای نشانگرهای سلولی خاص SASP و سایر عواملی است که منجر به ایجاد فیبروز می شود.
منطقی است که باور کنیم قبل از استفاده از PRP، پیری سلولی هدفمند میتواند ویژگیهای بازسازی اثربخشی درمان بیولوژیکی را با کاهش فاکتورهای SASP محلی بهبود بخشد.پیشنهاد شده است که گزینه دیگری برای بهبود نتایج درمان PRP و PPP برای بازسازی ماهیچه های اسکلتی، حذف انتخابی سلول های پیری با پاک کننده های پیری است.شکی نیست که نتایج تحقیقات اخیر در مورد تأثیر PRP بر پیری و پیری سلولی جذاب است، اما هنوز در مرحله اولیه هستند.بنابراین، ارائه هر گونه پیشنهادی در این زمان منطقی نیست.
(محتوای این مقاله تجدید چاپ شده است و ما هیچ تضمین صریح یا ضمنی برای صحت، اعتبار یا کامل بودن مطالب مندرج در این مقاله ارائه نمی دهیم و مسئولیتی در قبال نظرات این مقاله نداریم، لطفاً درک کنید).
زمان ارسال: مارس-01-2023