مفهومی که امروزه به عنوان PRP شناخته می شود برای اولین بار در دهه 1970 در زمینه هماتولوژی ظاهر شد.هماتولوژیست ها اصطلاح PRP را دهه ها پیش در تلاش برای توصیف پلاسمای بدست آمده از تعداد پلاکت ها بالاتر از مقادیر پایه در خون محیطی ابداع کردند.بیش از یک دهه بعد، PRP در جراحی فک و صورت به عنوان شکلی از فیبرین غنی از پلاکت (PRF) استفاده شد.محتوای فیبرین در این مشتق PRP به دلیل خاصیت چسبندگی و هموستاتیک آن ارزش زیادی دارد، در حالی که PRP دارای خواص ضد التهابی پایدار است و تکثیر سلولی را تحریک می کند.سرانجام، در حدود دهه 1990، PRP رایج شد و در نهایت، این فناوری به سایر زمینه های پزشکی منتقل شد.از آن زمان، این زیستشناسی مثبت به طور گسترده مورد مطالعه قرار گرفته و برای درمان آسیبهای اسکلتی عضلانی مختلف در ورزشکاران حرفهای به کار گرفته شده است، که بیشتر به توجه رسانهای گسترده آن کمک کرده است.PRP علاوه بر موثر بودن در ارتوپدی و پزشکی ورزشی در چشم پزشکی، زنان، اورولوژی و قلب، اطفال و جراحی پلاستیک کاربرد دارد.در سالهای اخیر، PRP به دلیل پتانسیل آن در درمان زخمهای پوستی، بازسازی اسکار، بازسازی بافت، جوانسازی پوست و حتی ریزش مو توسط متخصصان پوست مورد تحسین قرار گرفته است.
با توجه به اینکه PRP به طور مستقیم فرآیندهای بهبودی و التهابی را دستکاری می کند، آبشار شفا باید به عنوان مرجع معرفی شود.روند بهبودی به چهار مرحله زیر تقسیم می شود: هموستاز.التهاب؛تکثیر سلولی و ماتریکس و در نهایت بازسازی زخم.
1. بهبود بافت
یک آبشار بهبود بافت فعال میشود، فرآیندی که منجر به تجمع پلاکتها، تشکیل لخته، و ایجاد یک ماتریکس خارج سلولی موقت میشود (ECM. پلاکتها سپس به کلاژن و پروتئینهای ECM در معرض میچسبند و باعث حضور گرانولهای α در آزادسازی میشوند. مولکولهای فعال زیستی: پلاکتها حاوی انواع مولکولهای فعال زیستی از جمله فاکتورهای رشد، کموکاینها و سیتوکینها و همچنین واسطههای پیشالتهابی مانند پروستاگلاندینها، سیکلین پروستات، هیستامین، ترومبوکسان، سروتونین و برادی کینین هستند.
مرحله نهایی روند بهبودی به بازسازی زخم بستگی دارد.بازسازی بافت به شدت تنظیم می شود تا تعادل بین پاسخ های آنابولیک و کاتابولیک ایجاد شود.در طی این مرحله، فاکتور رشد مشتق شده از پلاکت (PDGF)، فاکتور رشد تبدیل کننده (TGF-β) و فیبرونکتین، تکثیر و مهاجرت فیبروبلاست ها و همچنین سنتز اجزای ECM را تحریک می کنند.با این حال، زمان بلوغ زخم تا حد زیادی به شدت زخم، ویژگیهای فردی و ظرفیت بهبودی خاص بافت آسیبدیده بستگی دارد و برخی عوامل پاتوفیزیولوژیکی و متابولیک میتوانند بر روند بهبودی تأثیر بگذارند، مانند ایسکمی بافت، هیپوکسی، عفونت. ، عدم تعادل فاکتور رشد و حتی بیماری های مرتبط با سندرم متابولیک.
یک ریزمحیط پیش التهابی که در روند بهبودی اختلال ایجاد می کند.برای پیچیده تر کردن مسائل، فعالیت پروتئاز بالایی نیز وجود دارد که از عملکرد طبیعی فاکتور رشد (GF) جلوگیری می کند.PRP علاوه بر داشتن خواص میتوژنیک، رگ زایی و کموتاکتیک، منبع غنی بسیاری از عوامل رشد، مولکول های زیستی است که ممکن است با کنترل التهاب تشدید شده و ایجاد محرک های آنابولیک، اثرات مضر را در بافت های ملتهب خنثی کند.با توجه به این ویژگی ها، محققان ممکن است پتانسیل زیادی در درمان انواع آسیب های پیچیده پیدا کنند.
2. سیتوکین
سیتوکین ها در PRP نقش کلیدی در دستکاری فرآیندهای ترمیم بافت و تنظیم آسیب های التهابی دارند.سایتوکاین های ضد التهابی طیف وسیعی از مولکول های بیوشیمیایی هستند که واکنش های سیتوکین های پیش التهابی را که عمدتاً توسط ماکروفاژهای فعال القا می شوند، واسطه می کنند.سایتوکاینهای ضد التهابی با مهارکنندههای سیتوکین خاص و گیرندههای سیتوکین محلول برای تعدیل التهاب تعامل دارند.آنتاگونیست های گیرنده اینترلوکین (IL)-1، IL-4، IL-10، IL-11 و IL-13 به عنوان سایتوکین های ضد التهابی اصلی طبقه بندی می شوند.بسته به نوع زخم، برخی از سیتوکینها مانند اینترفرون، فاکتور مهارکننده لوسمی، TGF-β و IL-6 میتوانند اثرات پیشالتهابی یا ضدالتهابی از خود نشان دهند.TNF-α، IL1 و IL-18 گیرنده های سیتوکین خاصی دارند که ممکن است اثرات پیش التهابی سایر پروتئین ها را مهار کنند [37].IL-10 یکی از قوی ترین سایتوکین های ضد التهابی است، می تواند سیتوکین های پیش التهابی مانند IL-1، IL-6 و TNF-α را کاهش داده و سیتوکین های ضد التهابی را تنظیم کند.این مکانیسم های ضد تنظیمی نقش مهمی در تولید و عملکرد سایتوکاین های پیش التهابی دارند.علاوه بر این، سیتوکینهای خاص ممکن است پاسخهای سیگنالی خاصی را تحریک کنند که فیبروبلاستها را تحریک میکنند، که برای ترمیم بافت حیاتی هستند.سیتوکین های التهابی TGFβ1، IL-1β، IL-6، IL-13 و IL-33 فیبروبلاست ها را برای تمایز به میوفیبروبلاست ها تحریک می کنند و ECM را بهبود می بخشند [38].به نوبه خود، فیبروبلاستها سیتوکینهای TGF-β، IL-1β، IL-33، CXC و CC کموکاینها را ترشح میکنند که با فعالسازی و بهکارگیری سلولهای ایمنی مانند ماکروفاژها، پاسخهای پیش التهابی را افزایش میدهند.این سلولهای التهابی نقشهای متعددی در محل زخم دارند، در درجه اول با ترویج پاکسازی زخم - و همچنین بیوسنتز کموکاینها، متابولیتها و فاکتورهای رشد، که برای بازسازی بافت جدید ضروری هستند.بنابراین، سیتوکین های موجود در PRP نقش مهمی در تحریک پاسخ های ایمنی با واسطه نوع سلول ایفا می کنند و حل فاز التهابی را هدایت می کنند.در واقع، برخی از محققین نام این فرآیند را «التهاب احیاکننده» گذاشتهاند که نشان میدهد فاز التهابی، علیرغم ناراحتی بیمار، با توجه به مکانیسمهای اپی ژنتیکی که سیگنالهای التهابی از طریق آن باعث ارتقای سلولی میشوند، یک گام حیاتی برای فرآیند ترمیم بافت برای رسیدن به یک نتیجه موفقیتآمیز است. پلاستیسیته
3. فیبرین
پلاکت ها دارای چندین عامل مرتبط با سیستم فیبرینولیتیک هستند که ممکن است پاسخ فیبرینولیتیک را تنظیم یا کاهش دهند.رابطه زمانی و سهم نسبی اجزای خونی و عملکرد پلاکتی در تخریب لخته همچنان موضوعی است که ارزش بحث گسترده در جامعه را دارد.ادبیات، مطالعات بسیاری را ارائه میکند که تنها بر پلاکتها تمرکز دارند، پلاکتهایی که به دلیل تواناییشان در تأثیرگذاری بر روند بهبودی شناخته شدهاند.علیرغم مطالعات برجسته متعدد، سایر اجزای هماتولوژیک مانند فاکتورهای انعقادی و سیستم فیبرینولیتیک نیز نقش مهمی در ترمیم موثر زخم دارند.طبق تعریف، فیبرینولیز یک فرآیند بیولوژیکی پیچیده است که بر فعال شدن آنزیم های خاصی برای تسهیل تجزیه فیبرین متکی است.پاسخ فیبرینولیتیک توسط نویسندگان دیگر پیشنهاد شده است که محصولات تخریب فیبرین (fdp) ممکن است در واقع عوامل مولکولی مسئول تحریک ترمیم بافت باشند، دنباله ای از رویدادهای مهم بیولوژیکی قبل از رسوب فیبرین و حذف از رگزایی، که برای بهبود زخم ضروری است.تشکیل لخته پس از آسیب به عنوان یک لایه محافظ عمل می کند که از بافت در برابر از دست دادن خون، تهاجم عوامل میکروبی محافظت می کند و همچنین ماتریکس موقتی را فراهم می کند که سلول ها می توانند از طریق آن در طول ترمیم مهاجرت کنند.این لخته به دلیل برش فیبرینوژن توسط پروتئازهای سرین و تجمع پلاکت ها در شبکه فیبری فیبرین متقابل است.این واکنش پلیمریزاسیون مونومرهای فیبرین را آغاز می کند، رویداد اصلی در تشکیل لخته خون.لختهها همچنین میتوانند به عنوان مخزن سیتوکینها و فاکتورهای رشد عمل کنند که پس از دگرانولاسیون پلاکتهای فعال آزاد میشوند.سیستم فیبرینولیتیک به شدت توسط پلاسمین تنظیم میشود و نقش کلیدی در ترویج مهاجرت سلولی، فراهمی زیستی فاکتور رشد و تنظیم سایر سیستمهای پروتئاز درگیر در التهاب و بازسازی بافت دارد.اجزای کلیدی در فیبرینولیز، مانند گیرنده فعال کننده پلاسمینوژن اوروکیناز (uPAR) و مهارکننده فعال کننده پلاسمینوژن-1 (PAI-1) شناخته شده است که در سلول های بنیادی مزانشیمی (MSCs)، یک نوع سلول تخصصی لازم برای بهبود موفقیت آمیز زخم بیان می شوند.
4. مهاجرت سلولی
فعال سازی پلاسمینوژن از طریق ارتباط uPA-uPAR فرآیندی است که مهاجرت سلول های التهابی را افزایش می دهد زیرا پروتئولیز خارج سلولی را افزایش می دهد.از آنجایی که uPAR فاقد حوزه های بین غشایی و درون سلولی است، پروتئین به گیرنده های مشترکی مانند اینتگرین و ویترئین برای تنظیم مهاجرت سلولی نیاز دارد.علاوه بر این، اتصال uPA-uPAR منجر به افزایش میل ترکیبی uPAR برای کانکسینها و اینتگرینهای زجاجیه شد و چسبندگی سلولی را تقویت کرد.مهارکننده فعال کننده پلاسمینوژن-1 (PAI-1) به نوبه خود سلول ها را جدا می کند و وقتی به uPA کمپلکس uPA-upar-اینتگرین روی سطح سلول متصل می شود، سلول ها را از بین می برد.
در زمینه پزشکی بازساختی، سلول های بنیادی مزانشیمی از مغز استخوان در زمینه آسیب شدید اندام بسیج می شوند و بنابراین ممکن است در گردش خون بیماران با شکستگی های متعدد یافت شوند.با این حال، در شرایط خاص، مانند نارسایی کلیه مرحله نهایی، نارسایی کبدی مرحله نهایی، یا در هنگام شروع رد پس از پیوند قلب، این سلول ها ممکن است در خون قابل تشخیص نباشند [66].جالب توجه است که این سلول های پیش ساز مزانشیمی (استرومایی) مشتق از مغز استخوان انسان را نمی توان در خون افراد سالم تشخیص داد [67].نقش uPAR در بسیج سلول های بنیادی مزانشیمی مغز استخوان نیز قبلاً پیشنهاد شده است، مشابه آنچه در بسیج سلول های بنیادی خونساز (HSC) رخ می دهد.ورابانی و همکاراننتایج نشان داد که استفاده از فاکتور محرک کلنی گرانولوسیت در موشهای دارای کمبود uPAR باعث شکست سلولهای بنیادی مزانشیمی شد و دوباره نقش حمایتی سیستم فیبرینولیتیک را در مهاجرت سلولی تقویت کرد.مطالعات بیشتر همچنین نشان داده اند که گیرنده های uPA لنگردار با گلیکوزیل فسفاتیدیل، چسبندگی، مهاجرت، تکثیر و تمایز را با فعال کردن مسیرهای سیگنال دهی داخل سلولی، به شرح زیر، تنظیم می کنند: مسیر فسفاتیدیل 4،5-بیس فسفات/بیس فسفات/2-3ktA و 4،5-bisphosphate/RK3kt. و چسبندگی کیناز (FAK).
سلول های بنیادی مزانشیمی اهمیت بیشتری را در زمینه بهبود زخم نشان داده اند.به عنوان مثال، موشهای دارای کمبود پلاسمینوژن تاخیر شدیدی را در رویدادهای بهبود زخم نشان دادند، که نشان میدهد پلاسمین نقش مهمی در این فرآیند دارد.در انسان، از دست دادن پلاسمین نیز می تواند منجر به عوارض بهبود زخم شود.اختلال در جریان خون می تواند به طور قابل توجهی از بازسازی بافت جلوگیری کند، که توضیح می دهد که چرا این فرآیندهای بازسازی در بیماران دیابتی چالش برانگیزتر هستند.
5. مونوسیت ها و سیستم های بازسازی
با توجه به ادبیات، بحث های زیادی در مورد نقش مونوسیت ها در بهبود زخم وجود دارد.ماکروفاژها عمدتاً از مونوسیتهای خون مشتق میشوند و نقش مهمی در پزشکی بازساختی دارند [81].از آنجایی که نوتروفیل ها IL-4، IL-1، IL-6 و TNF-[alpha] ترشح می کنند، این سلول ها معمولاً تقریباً 24-48 ساعت پس از آسیب به محل زخم نفوذ می کنند.پلاکت ها ترومبین و فاکتور پلاکت 4 (PF4) را آزاد می کنند، دو کموکاین که جذب مونوسیت ها و تمایز آنها به ماکروفاژها و سلول های دندریتیک را افزایش می دهند.ویژگی بارز ماکروفاژها انعطاف پذیری آنهاست، یعنی توانایی آنها در تغییر فنوتیپ ها و تمایز به انواع سلول های دیگر مانند سلول های اندوتلیال، که متعاقباً عملکردهای متفاوتی را در پاسخ به محرک های بیوشیمیایی مختلف در ریزمحیط زخم نشان می دهند.سلول های التهابی بسته به سیگنال مولکولی محلی که منبع محرک است، دو فنوتیپ اصلی M1 یا M2 را بیان می کنند.ماکروفاژهای M1 توسط عوامل میکروبی القا می شوند و بنابراین اثرات پیش التهابی بیشتری دارند.در مقابل، ماکروفاژهای M2 معمولاً توسط پاسخ نوع 2 تولید می شوند و دارای خواص ضد التهابی هستند که معمولاً با افزایش IL-4، IL-5، IL-9 و IL-13 مشخص می شوند.همچنین از طریق تولید فاکتورهای رشد در ترمیم بافت نقش دارد.انتقال از ایزوفرم های M1 به M2 عمدتاً توسط مراحل بعدی بهبود زخم انجام می شود، جایی که ماکروفاژهای M1 باعث آپوپتوز نوتروفیل می شوند و پاکسازی این سلول ها را آغاز می کنند.فاگوسیتوز توسط نوتروفیل ها زنجیره ای از رویدادها را فعال می کند که در آن تولید سیتوکین خاموش می شود، ماکروفاژها قطبی می شوند و TGF-β1 آزاد می شود.این فاکتور رشد یک تنظیمکننده کلیدی تمایز میوفیبروبلاست و انقباض زخم است که به رفع التهاب و شروع فاز پرولیفراتیو در آبشار بهبودی اجازه میدهد [57].پروتئین بسیار مرتبط دیگری که در فرآیندهای سلولی دخیل است، سرین (SG) است.مشخص شده است که این گرانولان ترشح شده توسط سلول های خونساز برای ذخیره پروتئین های ترشح شده در سلول های ایمنی خاص مانند ماست سل ها، نوتروفیل ها و لنفوسیت های T سیتوتوکسیک ضروری است.در حالی که بسیاری از سلولهای غیرخونساز سروتونین را سنتز میکنند، همه سلولهای التهابی مقادیر زیادی از این پروتئین را تولید میکنند و آن را برای تعامل بیشتر با سایر واسطههای التهابی از جمله پروتئازها، سیتوکینها، کموکاینها و فاکتور رشد در گرانولها ذخیره میکنند.به نظر میرسد زنجیرههای گلیکوزامینوگلیکان با بار منفی در SG برای هموستاز گرانول ترشحی حیاتی هستند، زیرا میتوانند به روشی خاص سلولی، پروتئینی و زنجیرهای GAG به اجزای گرانول باردار شده متصل شوند و ذخیرهسازی آنها را تسهیل کنند.با توجه به مشارکت آنها در PRP، Woulfe و همکاران قبلا نشان داده بودند که کمبود SG به شدت با تغییر مورفولوژی پلاکتی مرتبط است.نقص در فاکتور پلاکت 4، بتا ترومگلوبولین، و ذخیره سازی PDGF در پلاکت ها.تجمع ضعیف پلاکت و ترشح در شرایط آزمایشگاهی و ترومبوز در داخل بدن نقص را تشکیل می دهند.بنابراین محققان به این نتیجه رسیدند که به نظر می رسد این پروتئوگلیکان یک تنظیم کننده اصلی ترومبوز باشد.
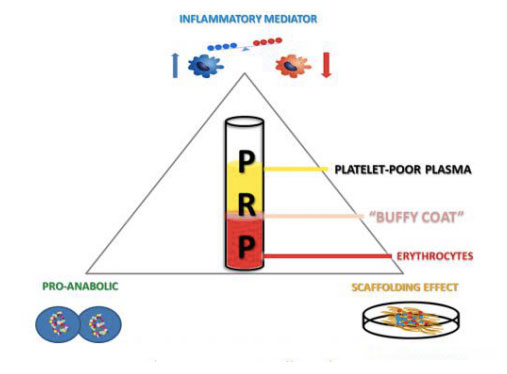
محصولات غنی از پلاکت را می توان با جمع آوری و سانتریفیوژ کردن خون کامل یک فرد، جدا کردن مخلوط به لایه های مختلف حاوی پلاسما، پلاکت ها، لکوسیت ها و لکوسیت ها به دست آورد.هنگامی که غلظت پلاکت ها بالاتر از مقادیر پایه باشد، رشد استخوان و بافت نرم می تواند با حداقل عوارض جانبی تسریع شود.استفاده از محصولات PRP اتولوگ یک بیوتکنولوژی نسبتاً جدید است که همچنان نتایج امیدوارکنندهای را در تحریک و بهبود بیشتر آسیبهای بافتی نشان میدهد.اثربخشی این رویکرد درمانی جایگزین را میتوان به تحویل موضعی طیف وسیعی از فاکتورهای رشد و پروتئینها، تقلید و حمایت از فرآیندهای بهبود فیزیولوژیکی زخم و ترمیم بافت نسبت داد.علاوه بر این، سیستم فیبرینولیتیک به وضوح تأثیر مهمی بر ترمیم کلی بافت دارد.علاوه بر توانایی آن در تغییر جذب سلولی سلولهای التهابی و سلولهای بنیادی مزانشیمی، فعالیت پروتئولیتیک را در نواحی بهبود زخم و در طول بازسازی بافتهای مزودرمی از جمله استخوان، غضروف و ماهیچه تعدیل میکند و بنابراین در بخش پزشکی اسکلتی عضلانی کلیدی است.
تسریع بهبودی هدفی است که بسیاری از متخصصان در زمینه پزشکی به دنبال آن هستند و PRP نشان دهنده یک ابزار بیولوژیکی مثبت است که همچنان به ارائه پیشرفت های امیدوارکننده در تحریک و هماهنگی رویدادهای بازسازی کننده ادامه می دهد.با این حال، از آنجایی که این ابزار درمانی پیچیده باقی میماند، بهویژه از آنجایی که تعداد بیشماری از عوامل فعال زیستی و مکانیسمهای برهمکنش مختلف و اثرات سیگنالدهی آنها را آزاد میکند، مطالعات بیشتری مورد نیاز است.
(محتوای این مقاله تجدید چاپ شده است و ما هیچ تضمین صریح یا ضمنی برای صحت، اعتبار یا کامل بودن مطالب مندرج در این مقاله ارائه نمی دهیم و مسئولیتی در قبال نظرات این مقاله نداریم، لطفاً درک کنید).
زمان ارسال: ژوئیه-19-2022